Verimix - Sınıf IIa Tıbbi Cihaz Ürün Kaydı Rehberi
Sınıf IIa Tıbbi Cihaz Nedir?
Sınıf IIa tıbbi cihazlar, orta riskli, belgelendirme gerektiren ve hasta güvenliği açısından kontrol mekanizmaları bulunan medikal ürünlerdir. Bu cihazlar genellikle kısa süreli veya invaziv olmayan uygulamalarda kullanılır ve insan sağlığı üzerinde belirli bir etkiye sahiptir, ancak hayati risk oluşturmazlar.
Sınıf IIa Tıbbi Cihazlara Örnekler:
- Diş dolgusu materyalleri
- Ultrason cihazları
- Cerrahi el aletleri
- Kontakt lensler
- İnsülin kalemleri
- Kan basıncı ölçüm cihazları
- Solunum maskeleri
Bu sınıftaki ürünler, genellikle hasta üzerinde geçici veya yüzeysel temas içeren tıbbi işlemlerde kullanılır. Ürünün sınıfı, kullanım süresi, temas şekli ve insan vücuduna etkisine göre belirlenir.
Sınıf IIa tıbbi cihazlar, Türkiye’de Ürün Takip Sistemi (ÜTS) kapsamında kayıt altına alınmakta ve bu sayede üretimden son kullanıcıya kadar izlenebilirlik, güvenlik ve denetim süreçleri etkin bir şekilde sağlanmaktadır.
Bu ürünlerin satışa sunulmadan önce ÜTS kaydının tamamlanmış olması gerekir.
İçindekiler
Sınıf IIa Tıbbi Cihaz ÜTS Ürün Kaydı Nasıl Yapılır?
1. Firma Kaydı
Ürün kaydı yapabilmek için öncelikle firmanın ÜTS’ye kayıtlı olması gerekir.
- Kayıt işlemleri ÜTS Uygulama adresinden yapılır.
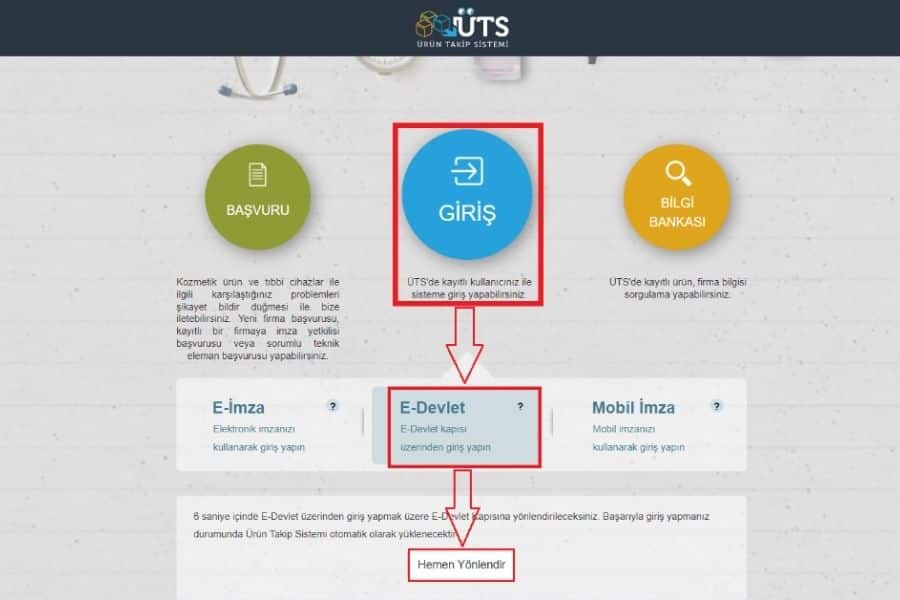
- Giriş için e-Devlet, e-imza veya mobil imza kullanılabilir.
- Firma unvanı, faaliyet alanı, adres, yetkili kişi bilgileri eksiksiz girilir.
- Başvuru tamamlandığında Sağlık Bakanlığı tarafından incelenir ve onaylanır.
Firma kayıt süreci için kılavuz: Firma Başvuru Kılavuzu (PDF)
2. Belge Kayıt İşlemleri
Sınıf IIa cihazlar için ürün kaydından önce belgelerin sisteme yüklenmesi zorunludur. Gerekli belgelerden bazıları:
- CE Sertifikası (Notified Body tarafından onaylanmış olmalı)
- Uygunluk Beyanı (Declaration of Conformity)
- Teknik dosya özet bilgileri
- Kullanım kılavuzu
- Kalite yönetim sistemi sertifikası (örneğin ISO 13485)
- Yetkili temsilcilik veya distribütörlük belgeleri (ithalatçılar için)
Belgeler elektronik ortamda yüklenir ve e-imza ile imzalanır. Bakanlık tarafından onaylandıktan sonra ürün kayıt adımına geçilir.
Belge başvuru rehberi: Belge Kayıt Başvurusu Hakkında PDF
3. Ürün Bilgilerinin Sisteme Girilmesi
Onaylı belgeler sonrasında, cihaz bilgileri ÜTS sistemine kaydedilir. Bu aşamada:
- Ürün adı ve ticari markası
- Model / versiyon / katalog numarası
- Ürün barkodu (GTIN / EAN)
- Üretici / ithalatçı bilgileri
- Kullanım amacı ve teknik özellikler
- Risk sınıfı (IIa) bilgisi
- Etiket bilgileri
girilir ve başvuru e-imza ile onaylanır.
4. Tekil Takip Bildirimi
Sınıf IIa cihazlarda çoğunlukla tekil ürün bildirimi zorunludur. Bu, her bir ürünün seri numarası veya lot numarası bazında sistemde takip edilmesi anlamına gelir.
- Ürün üretildiğinde veya ithal edildiğinde sisteme giriş bildirimi yapılır.
- Depo transferleri, satışlar, hastaneye sevkler veya iade işlemleri tek tek bildirilir.
- Ürün son kullanıcıya ulaştığında süreç tamamlanır.
Bu aşama, ürünün piyasada sahte veya kayıt dışı yollarla dolaşmasını önlemeye yardımcı olur.
Kullanılabilecek Resmî Kılavuzlar ve Bağlantılar
ÜTS sisteminde işlemleri doğru yapabilmek için Sağlık Bakanlığı’nın yayımladığı kılavuzlar büyük önem taşır:
- 📄 ÜTS Kullanıcı Kılavuzu (Uygulama)
- 📄 Belge Kayıt Başvurusu Hakkında Duyuru
- 🌐 ÜTS Resmî Web Sitesi
- 🌐 ÜTS Uygulama Giriş Ekranı
Önemli Notlar
- Ürün kaydı tamamlanmadan piyasaya arz yapılamaz.
- Belgelerde eksiklik veya yanlış bilgi olması halinde başvuru reddedilebilir.
- Her değişiklik (model, etiket, üretici vb.) için sistemde güncelleme yapılmalıdır.
- Ürün kayıt işlemleri genellikle yetkili kullanıcı hesabı üzerinden gerçekleştirilir.
Uyumlu, Güvenli ve İzlenebilir Bir Süreç
Sınıf IIa tıbbi cihazların Ürün Takip Sistemi (ÜTS) üzerinden kaydedilmesi, yalnızca yasal bir gereklilik değil; aynı zamanda hasta güvenliği, ürün kalitesi ve tedarik zinciri şeffaflığı açısından da kritik bir süreçtir.
Firma kaydı, belge yükleme, ürün bilgisi girişi ve tekil takip adımlarının eksiksiz tamamlanması, cihazların piyasaya güvenle arz edilmesini sağlar. Böylece üretici, ithalatçı ve distribütörler hem mevzuat uyumunu korur hem de olası denetim ve izleme süreçlerinde avantaj elde eder.
Düzenli ve doğru yürütülen ÜTS süreçleri, sağlık sektöründe güvenilirliği artırır ve kayıtlı her ürünün yaşam döngüsü boyunca izlenebilirliğini garanti altına alır.